Par Edouard H.
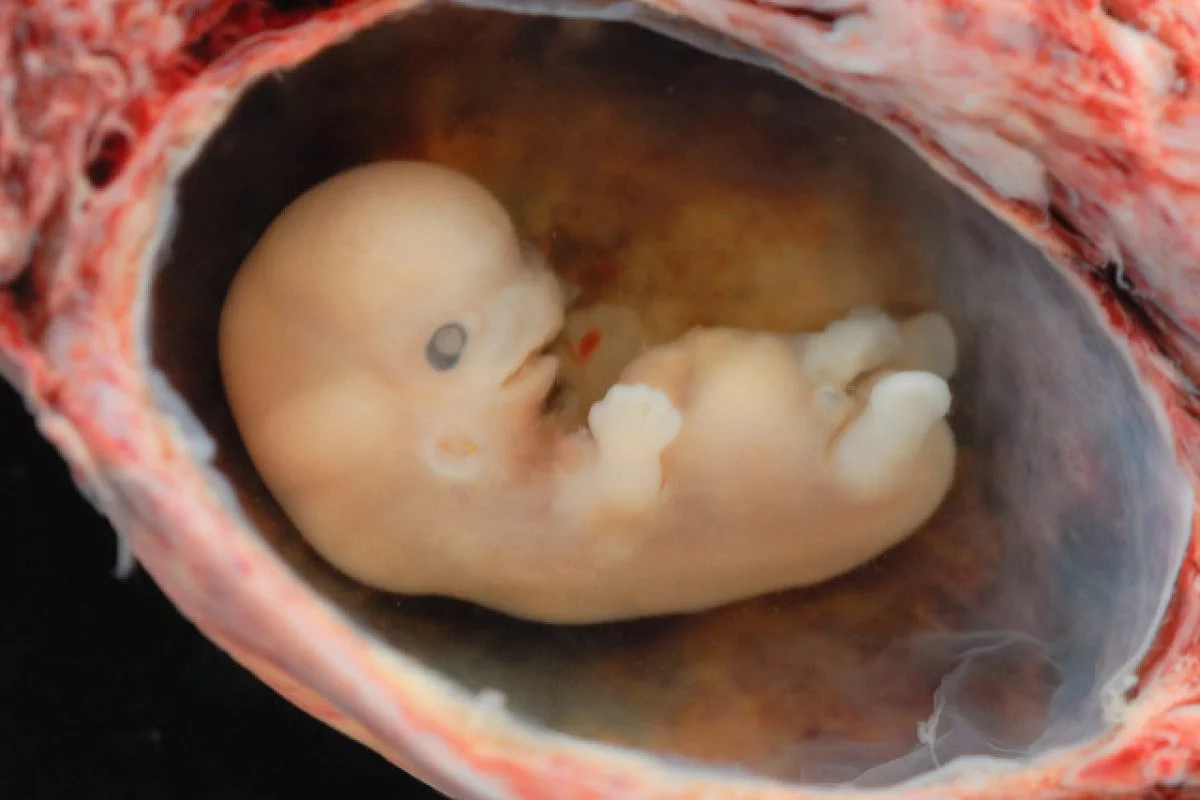
La nouvelle est tombée le 26 juillet dernier dans un article de la MIT Technology Review : une équipe de scientifiques américains ont modifié avec succès les gènes d’embryons humains à l’aide de CRISPR-Cas9. Une étude publiée dans le journal Nature le 2 juillet est venue donner de plus amples précisions sur l’exploit de l’équipe du Dr Shoukhrat Mitalipov de la Oregon Health & Science University.
La nouvelle a été reçue dans la presse avec un effroi considérable, et de nombreux appels à une prohibition ferme de ce type d’expérimentations ont été lancés. Y a-t-il raison de s’inquiéter ?
Les chercheurs ont ciblé une mutation dans un gène appelé MYBPC3 responsable de la cardiomyopathie hypertrophique qui est une maladie cardiaque héréditaire affectant 1 personne sur 500 dans le monde. Ce gène encode une protéine qui contribue à la maintenance des muscles cardiaques et à la régulation de ses contractions et décontractions.
Un gène MYBPC3 mutant entraine des symptômes qui peuvent entrainer un arrêt cardiaque. Bien que des traitements existent pour amoindrir les symptômes, il n’y a aucun moyen de s’attaquer à la cause génétique chez un patient1.
Dans l’étude de l’équipe menée par le Dr Shoukhrat Mitalipov, 58 embryons ont été utilisés et n’ont pas été implantés par la suite. La technologie CRISPR-Cas9, qui permet de faire des changements précis dans un génome de manière relativement aisée, n’avait précédemment été utilisée sur des embryons humains que dans 3 études menées par des équipes de chercheurs chinois2.
De grands progrès au niveau de l’innocuité de la modification génétique d’embryons
Les chercheurs de la Oregon Health & Science University se sont attaqués avec succès à 2 problèmes généralement associés à l’application de CRISPR-Cas9 pour de la thérapie génique chez les humains. Le premier risque est celui de créer des changements génétiques additionnels non voulus appelés mutations hors-cible. Les chercheurs n’ont trouvé aucune preuve de mutations hors-cible chez les embryons modifiés lors de leur expérimentation.
Le second risque est celui de créer des mosaïques, où différentes cellules dans l’embryon contiennent différentes séquences génétiques. Certaines cellules possèdent alors le génome corrigé, tandis que d’autres gardent le génome avec le gène MYBPC3 mutant.
Sur les 58 embryons utilisés par l’équipe du Dr Shoukhrat Mitalipov, un seul était une mosaïque. Pour arriver à ce résultat les chercheurs ont injecté les composants CRISPR–Cas9 dans les ovules au même moment où ils injectaient le sperme pour les fertiliser, alors que les précédentes études avaient fait des essais plus tard dans le développement de l’embryon.
Une technique de modification génétique efficace
Les chercheurs ont enquêté sur une situation où le père avait une copie mutante du gène MYBPC3, tandis que la mère n’avait que des copies non mutantes de ce gène. Lors d’une expérimentation de contrôle, sans surprise 47,4% des embryons (9 sur 19) n’ont pas hérité de la version mutante de MYBPC3. Lors de l’expérimentation avec injection de CRISPR-Cas9, 72.4% des embryons (42 sur 58) n’avaient que la version non mutante de MYBPC3.
Les embryons modifiés se sont développés in vitro de manière similaire aux embryons de contrôle, avec 50% d’entre eux qui ont atteint le stade de blastocyste où l’embryon contient différents types de cellules. La modification génétique n’a donc pas empêché le développement.
Paula Amato, endocrinologue de la reproduction à la Oregon Health & Science University, a exprimé dans le Washington Post son grand enthousiasme à l’idée de pouvoir corriger des maladies avant la naissance. Bien que le diagnostic génétique pré-implantatoire existe pour sélectionner des embryons sains, elle regrette que la technique ne fonctionne pas dans tous les cas.
Elle raconte que malgré 3 cycles de fécondation in vitro, tous les ovocytes d’une de ses patientes étaient porteurs de la mutation génétique qui entraîne des maladies. Avec la technologie de correction génétique du Dr Shoukhrat Mitalipov, elle explique qu’ils « auraient pu sauver quelques embryons ».
Des cris d’alarme qui n’ont pas lieu d’être
Bien que les travaux du Dr Shoukhrat Mitalipov soient extrêmement prometteurs, la recherche sur la modification génétique d’embryons humains n’en est encore qu’à ses débuts. De nombreuses autres études scientifiques devront être menées pour confirmer tant l’innocuité que l’efficacité de l’édition génétique d’embryons avant qu’une implantation en vue de grossesse puisse être envisagée. Il serait en effet aujourd’hui irresponsable de faire naître des enfants par cette technique.
Mais une fois que l’édition génétique d’embryons sera rendue pleinement sure et efficace, quelle justification rationnelle y aura-t-il pour retirer ce choix aux couples désirant des enfants ? Qu’y a-t-il de mauvais et de contraire à l’éthique dans le fait que des parents souhaitent ne pas transmettre de terribles maladies génétiques à leurs enfants ?
Une déclaration condamnant ces technologies reproductives a été publiée le 3 août par un groupe d’organisations mené par la Stanford University. Cette déclaration est intéressante car on peut y découvrir plusieurs arguments justifiant le rejet.
Ainsi on peut lire que la modification génétique d’embryons pourrait être dangereuse pour les enfants à naître car elle éroderait « les instincts parentaux d’acceptation inconditionnelle ». Or rien ne permet de dire que les parents utilisant cette technologie feront preuve de moins d’amour inconditionnel : corriger quelques défauts génétiques d’un embryon n’empêche aucunement d’accepter et d’aimer pleinement l’enfant une fois né, peu importe ses traits.
Les auteurs de la déclaration expliquent aussi que « le malaise qu’on ressent le plus profondément est conceptuel : le sentiment que lorsqu’on identifie certains individus et leurs traits comme « indésirables », on fait l’expérience d’une perte collective de notre humanité ». L’erreur faite ici est une grave confusion entre le fait de rejeter une maladie, et le fait de rejeter les individus existant porteurs de cette maladie. Chercher à faire naître des enfants sains sans gène mutant MYBPC3 n’implique en aucun cas de rejeter les individus existant aujourd’hui et souffrant de cardiomyopathie hypertrophique.
Arriver à se débarrasser entièrement de maladies génétiques dramatiques ne serait pas une « perte collective de notre humanité » mais bien au contraire un immense progrès. La loterie génétique naturelle peut être extrêmement cruelle et il n’y a aucun vice à la combattre grâce à la science pour améliorer la santé des enfants à naître.
L’expérimentation du Dr Shoukhrat Mitalipov est porteuse d’espoir, et il n’y a pas lieu de créer des législations d’exception liberticides parce que certains ressentent au fond d’eux même un sentiment de dégoût irrationnel.
- Maron, B. J. (2002). Hypertrophic cardiomyopathy: a systematic review. Jama, 287(10), 1308-1320. ↩
- Liang, P., Xu, Y., Zhang, X., Ding, C., Huang, R., Zhang, Z., … & Sun, Y. (2015). CRISPR/Cas9-mediated gene editing in human tripronuclear zygotes. Protein & cell, 6(5), 363-372 ; Kang, X., He, W., Huang, Y., Yu, Q., Chen, Y., Gao, X., … & Fan, Y. (2016). Introducing precise genetic modifications into human 3PN embryos by CRISPR/Cas-mediated genome editing. Journal of assisted reproduction and genetics, 33(5), 581-588 ; Tang, L., Zeng, Y., Du, H., Gong, M., Peng, J., Zhang, B., … & Liu, J. (2017). CRISPR/Cas9-mediated gene editing in human zygotes using Cas9 protein. Molecular Genetics and Genomics, 292(3), 525-533. ↩

Les réactions négatives, de non scientifiques, mais aussi de scientifiques, sont les séquelles du fatalisme qui a accompagné l’humanité pendant des siècles. Les enfants atteints ne vivaient pas, et participaient à la mortalité infantile de toutes causes.
Le problème d’aujourd’hui est que ces enfants survivent, un certain temps, avec cette menace.
Si la science permet le dépistage dès la conception, de la maladie génétique, elle permettra aux parents de recourir à une IVG.
Les réserves ou les refus seront, bien entendus, possibles, mais les décisions se prendront en connaissance de cause.
Ce qui me semble contestable, ce n’est pas la volonté de s’attaquer à des maladies génétiques, mais les conditions dans lesquelles s’effectue cette attaque.
Catholique convaincu, promoteur de la Doctrine Sociale de l’Église (qui se fonde sur la foi ET la raison, et dont je crois qu’il s’agit d’un trésor pour l’humanité), j’adhère pleinement au principe de base de ladite doctrine, le principe personnaliste, selon lequel toute personne humaine dispose, de la conception à la mort naturelle, d’une incomparable et inconditionnelle dignité. C’est ce principe qui me conduit à être, comme vous, cher Édouard, un “anarchiste libéral”. En effet, d’après l’Église catholique (Constitution Gaudium et spes), “la dignité de l’homme exige donc qu’il agisse selon un choix conscient et libre, mu et déterminé par une conviction personnelle, et non sous le seul effet de pulsions instinctives ou d’une contrainte extérieure”. Les conditions dans lesquelles sont effectués les recherches que vous décrivez ne me semblent pas respectueuses de la dignité des embryons (à mes yeux, personnes humaines à part entière) sur lesquels elles sont effectuées.
Il n’est pas question, me concernant, de “dégoût irrationnel”. Ceci dit, je ne crois pas que l’interdiction de telles recherches soit la solution : dans le respect du principe personnaliste, et sans vouloir me poser en “donneur de leçons” (à quel titre y serais-je autorisé ?) je pense prioritaire de faire connaître la DSÉ et ses conséquences logiques. Tant qu’une large partie de la population considèrera qu’un embryon n’est pas une personne humaine à part entière, disposant de droits naturels imprescriptibles, je ne pourrai pas être d’accord avec elle sur la légitimité des recherches exposées dans cet article ou sur celle de l’avortement.
Bien que je ne sois pas du tout d’accord avec l’idée que l’embryon est une personne j’apprécie la manière dont vous avez tourné votre message. Effectivement tout est là. Embryon personne ou pas? Les personnes je peux avoir des interactions avec elles. J’ai personellement jamais réussi à avoir d’interraction avec un embryon. Un Feotus, on peut se poser la question. Il écoute dans le ventre de mère. Il bouge, il y a un début d’interraction.
J’ai plus d’empathie pour un singe ou un rat que pour un embryon. Et je ne serai pas du tout surpris que la souffrance des singes et rats sur qui on fait des expériences est bien plus réelle que celle des embryons. Tout ça pour dire que la vision religieuse de la chose est très discutable: Pourquoi un embryon est il plus sacré qu’un animal bien né vivant et capable de souffrir? Pourquoi un embryon au stade cellule oeuf mérite plus de respect qu’une bactérie? Tant qu’on est au stade de morula peut on vraiment parler d’individu sachant qu’on pourrait parler d’autant d’individus qu’il y a de cellules (jusqu’à 64). Le concept d’individu est vraiment très très flou au stade embryonnaire. Adpoter une position arrêtée comme de l’église est, me semble t’il assez peu rationnel. Ca ne correspond pas vraiment à des données objectives mais à un sentiment (l’enfant sacré etc…). Si on creuse et qu’on demande le pourquoi des choses je ne suis jamais convaincu.
je suppose que si l’on n’est pas croyant, dans l’absolu, le concept de “personne” n’existe pas, mais qu’il est relatif (société, famille etc…).
De l’autre côté, l’Eglise propose une vision globale centrée sur l’être humain comme hypothétiquement une “personne” dans l’absolu du début à la fin (première cellule à la mort ?).
Vis à vis de votre point de vue, la “personne” se définirai par ses interactions avec le monde ? Ou bien pré-existe t’elle à ces interactions ?
Je n’ai pas dit que ça la définit. J’ai dit que c’est un critière discriminant. Tous les êtres vivants avec lesquels je peux avoir une interraction ne sont pas des personnes, (j’ai des interractions avec les chiens par exemple). En revanche je ne vois pas comment on pourrait appeler personne un être vivant avec lequel il est impossible d’interragir. Un être humain privé d’absolument tous ses sens est il encore un être humain? on peut le penser au regard de son ADN. Néanmoins l’impossibilité totale d’interragir avec lui si on le rencontre risque d’en faire rapidement un légume pour quiconque le croise…
Ne me semblent pas respectueuses de la dignité des embryons? En quoi? Laisser des bébés naître avec des malformations serait digne pour les bébés? Vous êtes ignoble, car ce que vous ne dites pas c’est que vous pensez que l’on a PAS le droit d’aller contre la volonté de Dieu. Or même s’il existe, on sait bien qu’il n’intervient JAMAIS dans nos existences et que seul le hasard perturbe la génétique, créant des malformations dommageables pour les organismes atteint.
une personne humaine à part entière, disposant de droits naturels imprescriptibles? Le droit de naître pour mourir aussitôt car incapable de fonctionner correctement? Vos arguments sont grotesques!
Guérir les bébés avant qu’ils naissent serait horrible? J’ai du mal à comprendre l’éthique des opposants à cette thérapie, quelle justification peuvent-ils apporter à leur ignoble rejet? Que l’on aille à rebours de la nature. Mais cette nature déraille, il faut donc que l’on intervienne pour sauver des vies!
de “réparer” à “améliorer”, il y a moins d’un pas. Il faut considérer le problème dans l’ensemble, pas prendre des cas extrêmes et réagir de façon épidermique.
Avez vous, par hasard, vu “bienvenu à Gatacca” ?
Il est évident qu’en matière d’éthique nous sommes dans le cas d’un continuum où nous avons du mal à savoir si nous sommes dans la zone noire, grise foncée, claire ou blanche; c’est encore plus tenu que le “pas” que vous cité.
Thierry Jallas dans son commentaire met en avant la dignité humaine qui veut que l’individu humain soit un but et non un moyen. Dans cette optique soigner un embryon avant sa naissance n’a pas moins de justification que de le soigner après.
Par contre comme vous le remarquez “améliorer” c’est adapter l’homme à des conditions sociales (notamment) et donc en faire un moyen.
Je crois qu’il y a un procès d’intention, la possibilité de guérir les “défauts” — qui pour certains n’en sont pas du fait du dogme de l’infaillibilité divine — ouvrant celle du choix par les parents d’améliorations moins fondamentales — qui pour les mêmes seraient des perversions inconséquentes de la volonté divine.
L’idée serait que par nature, l’Homme fait le mal et le Divin fait le bien. Je m’interroge sur comment dans ce cas le Divin a pu créer l’Homme, mais ma culture religieuse est très lacunaire.
C’est une conception de l’action divine qui voudrait que toute chose, tous phénomènes soient le résultat d’une volonté Divine. Si l’enfant est malade et décèdera à court terme, peut être dans de grande souffrance ce serait une “décision”, une “action” divine.
Donc la dureté, les calamités, les maladies qui nous accablent seraient d’origine divine. C’est un Dieu bien terrible que voilà. Devant ce Dieu il n’y aurai pour l’humanité que la voie de la piété ou de la révolte.
Je suppose que l’on peut de façon moins terrible estimer que si Dieu a créé l’univers avec sa part de calamité, dont la maladie qui peut affecter un enfant; il ne décide pas ponctuellement que tel ou tel enfant va mourir. Auquel cas agir sur la maladie n’est pas contrecarrer la volonté divine.
Infaillibilité divine? Tout le monde sait que Dieu n’intervient JAMAIS dans la vie des hommes et l’Univers!
Article remarquable en tout point qui prêche un convaincu. Excellentes analyses et argumentaires.
Tant qu’il s’agit de guérir ou prévenir des maladies il est effectivement difficile de trouver des raisons valables de s’opposer. Les craintes qui s’expriment concernent avant tout les autres applications de ces technologies. L’eugenisme est un risque non négligeable. Le débat est loin d’être évident.
Je pense qu’il faut laisser ceux qui sont contre ces pratiques ne pas les utiliser s’ils en ont envie. Par contre, il faut laisser ceux qui en ont besoin (évaluation de la nécessité par un ou plusieurs professionnels de santé compétent) y avoir recours.
Peu importe ce qu’en pense Thierry jallas, les cathos, les musulmans, le père Noël… bref laisser les gens faire à leur guise. Quand à ceux qui croient qu’on peut améliorer un être humain uniquement grâce à la génétique, je leur conseille de se renseigner un peu plus sur l’aqcuis, l’epigenetique, l’importance du cadre social etc… qui sont bien plus important que la génétique lors de la constitution d’un individu
Techniquement, c’est de l’eugénisme puisque l’on cherche à améliorer le patrimoine génétique de notre espèce.
Anticipons plusieurs problèmes envisageables à long terme :
– La manipulation génétique peut se faire selon des objectifs politiques / idéologiques.
– La possibilité d’y avoir recours peut muter en obligation sous le poids d’une forte pression sociale.
– Elle peut aussi finir par figer des castes sociales si elle dépend de moyens financiers.
– En éradiquant les maladies génétiques nous pourrions obtenir un effet inverse de celui désiré par l’eugénisme ; à savoir une détérioration de notre patrimoine génétique en éradiquant le travail de la sélection dite naturelle.
– À terme n’allons pas finir par annihiler toute forme de personnalité si nous entrons sur le chemin de la chasse aux défauts ? Pour peu qu’il existe un gêne dédié à la servilité ou à l’homosexualité par exemple, où nous conduiront ces découvertes ?
Ce n’est pas non plus comme si nous maîtrisions parfaitement notre sujet, que ce soit d’un point de vue scientifique ou politique. Je crois qu’à ce stade avoir un avis arrêté sur la question reste prématuré.
D’où sortez vous cette aberration ? Bien sûr que Dieu intervient dans l’existence humaine. Il est en perpétuelle interaction avec nous