Par Le Minarchiste.

Vous avez peut-être récemment entendu parlé de la forte hausse de prix du médicament Epipen mise en place par Mylan au cours des dernières années. Le produit se vend maintenant $600 aux États-Unis comparativement à $100 en 2009.
En fait, Epipen n’est rien d’autre qu’un injecteur d’épinéphrine (appelée aussi adrénaline). L’épinéphrine est une molécule que l’on synthétise depuis 1906 et ne coûte qu’environ 10 centimes par dose à produire. C’est l’injecteur qui constitue la principale technologie défendue par Mylan. Pourquoi n’y a-t-il pas davantage de concurrence dans ce créneau ? Pourtant, l’Europe ne compte pas moins de 8 versions concurrentes de ce produit.
Des concurrents bloqués
En 2009, Teva a annoncé qu’elle voulait vendre ses propres Epipen aux États-Unis. Puis, l’entreprise a été poursuivie par Mylan puisque cette dernière affirme détenir un brevet sur le concept d’auto-injecteur. Néanmoins, Teva a tout de même réussi à amener le produit devant la FDA, qui n’a toujours pas donné son approbation à ce jour !
En 2010, l’entreprise Sandoz (division de Novartis) a aussi tenté de commercialiser une version générique d’Epipen, mais ce produit demeure coincé dans une poursuite reliée au brevet, comme ce fut le cas pour Teva. Il est clair que Mylan utilise le système légal pour intimider ses concurrents potentiels, même si elle sait que ses chances de l’emporter sont minces. Ces poursuites permettent aussi de gagner du temps en gardant les concurrents hors du marché un peu plus longtemps.
En juin 2016, une compagnie du nom d’Adamis a décidé de contourner le brevet de Mylan en commercialisant plutôt des seringues pré-remplies d’épinéphrine que les patients pourraient s’injecter eux-mêmes, mais comme vous l’aurez deviné, la FDA a refusé cette idée.
Le seul produit encore sur le marché à avoir réussi à franchir les portes de la FDA est Adrenaclick (anciennement appelé Twinject). Cependant, sa part de marché est très limitée à ce jour, malgré le fait qu’il coûte significativement moins cher qu’Epipen.
La tentative de concurrence de Sanofi
En 2011, l’entreprise Sanofi tentait de faire approuver sa version générique, nommée E-Cue, mais la FDA l’a initialement refusée car elle n’aimait pas ce nom. Sanofi a donc changé le nom pour Auvi-Q, que nous avons connu au Canada sous la marque Allergec. C’est d’ailleurs ce produit fantastique que mon allergologue a prescrit à mes deux jeunes enfants.
Comble de malheur, en 2015 Sanofi a procédé à un rappel volontaire de tous les Auvi-Q/Allergec suite à un problème potentiel de dosage. Les pharmaciens pouvaient alors les remplacer sans frais par une Epipen. Puis, en 2016, Sanofi décide d’abandonner les droits de commercialisation de ce médicament, laissant un monopole à Mylan. L’entreprise détentrice du brevet, nommée Kaléo (anciennement Intelligect), doit maintenant trouver un nouveau partenaire pour le commercialiser.
Pourtant, seulement 26 cas de défaillance potentielle furent rapportés, comparativement à 2,8 millions d’unités vendues en Amérique du Nord depuis janvier 2013. Aucun de ces 26 cas n’a entraîné un décès. Au Canada, durant les deux années au cours desquelles Allergec a été commercialisé, seulement 10 incidents ont été signalés, comparativement à 34 pour Epipen. On constate donc que les deux produits sont sûrs.
Les laboratoires plus riches ont les moyens de tenir
Pourquoi alors Sanofi a-t-elle abandonné ce produit ? Sans doute en raison des risques de poursuites, des coûts potentiels pour vérifier s’il existe bel et bien un problème de dosage, mais aussi pour son incapacité à gagner des parts de marché suffisantes pour réaliser un profit intéressant.
L’une des raisons pour lesquelles Adrenaclick et Auvi-Q n’ont jamais réussi à obtenir une part de marché convenable aux États-Unis est que les médecins inscrivent souvent « Epipen » sur leur carnet de prescriptions au lieu d’écrire « auto-injecteur d’épinéphrine », ce qui empêche les pharmaciens de vendre les alternatives moins dispendieuses (Epipen bénéficie d’une règle spéciale à cet égard aux États-Unis et peut-être au Canada aussi). C’est l’une des raisons principales expliquant pourquoi les concurrents ont tant de difficulté à percer ce marché, tant au niveau des produits originaux que des génériques.
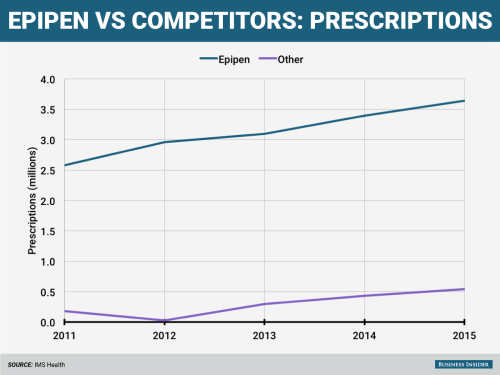
Et comme Mylan utilise habilement le système de justice pour faire grimper les coûts fixes, tout comme le font les procédures longues et coûteuses de la FDA, plusieurs concurrents jugent que le jeu n’en vaut pas la chandelle. Il est aussi possible que Mylan soit derrière le rappel de Auvi-Q/Allergec et que cela ait effrayé Sanofi.
Et un peu de lobbying ?
Il y a aussi un autre moyen par lequel Epipen s’assure une part de marché supérieure. En décembre 2012, la National Association of State Boards of Education a lancé une initiative visant à aider les écoles à développer des politiques concernant les chocs anaphylactiques. Curieusement, la mère de la PDG de Mylan, Heather Bresch, est devenue présidente de cette association en 2010 ! Epipen a fait de généreux dons à cette association par la suite. À l’époque, le père de Mme Bresch, un dénommé Joe Manchin, était gouverneur de l’État de Virginie. En 2013, suite à un intense lobby de la part de Mylan, le Congrès a adopté le School Access to Emergency Epinephrine Act, qui prévoyait entre autres du financement fédéral pour que les écoles achètent des injecteurs d’épinéphrine.
Je serais surpris que ces lois et initiatives aient spécifiquement mentionné la marque Epipen (bien que cela soit possible), mais il n’en demeure pas moins qu’étant donné ses alliés politiques, Mylan était en excellente position d’obtenir ces ventes.
Le marché américain verrouillé par la FDA
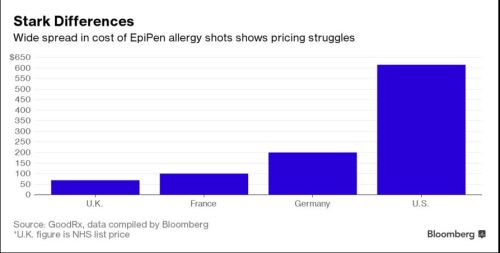
Au Royaume-Uni, la dose d’Epipen se vend $69. Il y a au moins deux autres concurrents : Jext et Emerade. En 2015, l’entreprise canadienne Valeant a abandonné la commercialisation d’Emerade aux États-Unis face aux exigences de la FDA. Quant à Alk-Abello, elle voudrait bien lancer Jext aux États-Unis, mais l’entreprise ne sait pas si cela en vaut la peine considérant les coûts de réglementation et la domination d’Epipen.
L’autre chose à considérer est que la plupart des assureurs ne paient pas les $608 exigés par Mylan. Les assureurs vont négocier des rabais, souvent via l’entreprise de leurs fournisseurs de service de gestion des prescriptions (aka PBMs). Ainsi, il se peut bien que les PBMs réussissent à obtenir un prix de $420 par Epipen, conservent une portion de l’escompte et revendent le produit $500 à un assureur. L’Affordable Care Act stipule que des rabais minimum doivent être consentis aux assureurs.
Face à ces « rabais » de plus en plus généreux, les laboratoires pharmaceutiques ont avantage à augmenter leur prix au détail, qui leur permet de maintenir une bonne marge de profit. Ainsi, Mylan indiquait avec raison que le prix de vente d’Epipen net du rabais aux PBMs a beaucoup moins augmenté que le prix au détail. On constate donc que personne ne paie le même prix pour l’Epipen, ce qui rend l’établissement d’un marché concurrentiel très difficile. Merci ACA…
Conclusion
Le cas de l’Epipen illustre presque toutes les failles majeures du système de santé américain : abus du système de brevet, abus du système légal, réglementation trop lourde, ingérence politique, etc. Le gouvernement devrait d’abord concéder que le concept d’auto-injecteur d’épinéphrine ne peut pas être breveté car cela est trop général. Puis il devrait abolir la règle empêchant les pharmaciens de proposer une alternative moins dispendieuse à Epipen. Quant aux malversations politiques des parents de la PDG de Mylan, elles découlent de problèmes plus profonds affectant le gouvernement américain, et qui nécessiteraient des changements dans la constitution pour être réformés.
Ce qui est le plus malheureux est que la gauche en profite pour utiliser cet exemple pour dénoncer les supposés « excès du capitalisme débridé ». Une simple analyse des faits démontre que les causes sous-jacentes à cette problématique découlent directement des politiques gouvernementales et d’un manque de capitalisme !
Quelques sources :
http://slatestarcodex.com/2016/08/29/reverse-voxsplaining-drugs-vs-chairs/
https://en.wikipedia.org/wiki/Epinephrine_autoinjector#History
—





Il faudrait une profonde réforme du système des brevets et des AMM à défaut de supprimer totalement , par exemple limitation des durées des brevets et interdiction de redéposer un brevet pour un produit à peu près identique dans sa forme et son fond.Pour les AMM une mise sur le marché hors AMM pour une durée limitée et une réforme de la procédure devra être sérieusement envisagée sur le modèle Japonais…
Les commentaires sont fermés.